Jetzt schon für den Rare Diseases Run 2026 anmelden
und 44 Vereine unterstützen!
Anmeldung Rare Diseases Run 2026
Was ist STXBP1?
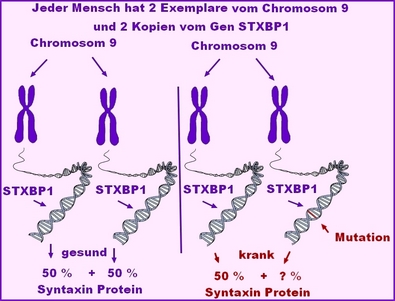
Das STXBP1-RD wird durch Veränderungen des STXBP1-Gens auf Chromosom 9 verursacht. STXBP1 ist eine seltene genetische Erkrankung, die ca. 1:30.000 Neugeborene betrifft. STXBP1 (Syntaxin-Bindung Protein 1) spielt eine Schlüsselrolle bei der Freisetzung von Neurotransmittern aus synaptischen Vesikeln. Es unterstützt das Verschmelzen der Vesikel mit der präsynaptischen Membran, indem es mit Syntaxin interagiert. Syntaxin-1 vermittelt das Andocken und die Verschmelzung von synaptischen Vesikeln mit der präsynaptischen Membran, indem es den Aufbau des SNARE-Komplexes erleichtert. Zusammen mit anderen SNARE-Proteinen (z. B. SNAP-25 und VAMP2/Synaptobrevin) bildet Syntaxin-1 einen SNARE-Komplex, der die Membranen der Vesikel und der präsynaptischen Membran fest miteinander verschmilzt, um Exozytose und die Freisetzung von Neurotransmittern zu ermöglichen. Störungen in STXBP1 können die Funktion von Syntaxin-1 indirekt beeinträchtigen und so die Neurotransmitter-Freisetzung sowie neuronale Signalübertragung beeinflussen. Eine STXBP1-assozierte Störung wird in der Regel durch De-novo-Mutationen im STXBP1-Gen verursacht.
Ein Buch für Eltern
Welche zentralen Inhalte bietet dieses Buch speziell für Eltern eines Kindes mit STXBP1-bezogenen Erkrankungen?
Das Buch "STXBP1-Enzephalopathie" soll Eltern mit einem STXBP1–Kind helfen, die Genmutation und den genetischen Befund zu verstehen. Es bietet in mehreren Bereichen Unterstützung und Informationen zu Therapien sowie zu aktuellen Forschungsansätzen.
Ergänzend enthaltene Ressourcen umfassen eine praxisnahe Checkliste für Arztbesuche, ein Glossar zentraler Begriffe sowie Empfehlungen zu begleitenden Therapien und rehabilitativen Angeboten. Die Inhalte richten sich an deutschsprachige Familien aus Deutschland, der Schweiz, Österreich und dem deutschsprachigen Belgien. Das Buch kann kostenfrei von Eltern mit einem STXBP1–Kind angefordert werden.
Zensus: weltweite STXBP1-Patienten Zählung
Wie viele STXBP1-Patienten werden global im Zensus Q4 2025 erfasst? (Update Q4 2025 vom 27. Dezember)
Im Dezember 2025 wurden weltweit die Fälle der STXBP1-Patienten gezählt. Die gemeldeten bekannten Fälle belaufen sich auf 1.479. Da jedoch sicherlich eine nicht diagnostizierte Population besteht, ist von einer höheren tatsächlichen Prävalenz auszugehen.
In der Europäischen Union leben gemäß aktueller Schätzungen 548 Patienten mit einer STXBP1-Diagnose. In Deutschland sind es mittlerweile 109. Die Zahlen verdeutlichen die erhebliche Untererfassung und den Bedarf an verstärkter Aufklärung, Diagnostik sowie standardisierten Erfassungs- und Meldestrukturen, um eine verlässlichere Datengrundlage für Forschung, Versorgung und Ressourcenplanung zu schaffen.
Symptome
Welche typischen Symptome treten bei STXBP1-bezogenen Erkrankungen auf?
Mutationen in STXBP1 können schwere neurologische Störungen verursachen, häufig schon im frühen Kindesalter, z. B. Epilepsie, Entwicklungsverzögerung, kognitive Einschränkungen und Sprach- bzw. Motorikprobleme. Epileptische Anfälle können verschiedene Formen annehmen und sind manchmal schwer behandelbar.
Die Entwicklungsverzögerung führt oft zu einer geistigen Behinderung. Zu den Berwegungsstörungen gehören ein niedriger Muskeltonus (Hypotonie), Koordinationsprobleme (Ataxie), Tremor (Zittern), Dystonie (Muskelverkrampfungen), oder Spastik. Betroffene entwickeln nur begrenzte oder gar keine Sprachfähigkeiten. Manche Kinder zeigen autistische Züge und Verhaltensauffälligkeiten und können ihre Lautstärke nur schwer regulieren. Zudem gibt es Kinder mit zerebraler visueller Beeinträchtigung (CVI, cortical visual impairment), obwohl die Augen gesund sind; die visuelle Reizverarbeitung funktioniert nicht optimal.
Sudden Unexpected Death in Epilepsy (SUDEP) kann eine seltene, aber ernsthafte Todesursache bei Epilepsie sein. Auch bei STXBP1-bedingten Epilepsien besteht ein erhöhtes SUDEP-Risiko, wobei die genauen Mechanismen noch erforscht werden. Sich über Sudep zu informieren ist wichtig, da Prävention, Risikoreduzierung und frühzeitige Therapie helfen können.
Die Symptome bei STXBP1-RD sind extrem unterschiedlich. Sie reichen von mild bis schwer, mit einer großen Bandbreite an neurologischen Problemen. STXBP1-Zwillinge sind extrem selten, aber Studien zeigen, dass selbst eineiige Zwillinge mit der STXBP1-Mutation unterschiedliche Krankheitsverläufe (Phänotypen) aufweisen können. Das unterstreicht die Komplexität der STXBP1-RD und betont individuelle Unterschiede, obwohl Patienten dieselbe genetische Ursache teilen.
Diagnose
Welche genetische Untersuchung ist notwendig, um eine STXBP1-Variante als Ursache der Symptome nachzuweisen?
Die Diagnose einer STXBP1-RD erfolgt über Gentests und ist überwiegend de novo, also nicht vererbt. Mosaizismus-Veränderungen in der Vererbung sind bekannt. Diese Mosaizismus-Veränderungen können die Vererbung beeinflussen.
Varianten im Gen STXBP1 können autosomal-dominant wirken. Schon eine heterozygote Mutation (ein mutiertes Allel der beiden Allele) kann ausreichend sein, um die Krankheitssymptomatik mit klinischen Merkmalen auszulösen.
Die Diagnose wird in der Regel durch eine Kombination aus klinischen Merkmalen, familiärer Vorgeschichte und genetischen Tests gestellt.
Genetische Sequenzierung des STXBP1-Gens (z. B. Next-Generation Sequencing, panelbasierte Tests oder Exom-Sequenzierung) werden zur Identifizierung von pathogenic, wahrscheinlich pathogenic Varianten oder VUS (Variants of Uncertain Significance) eingesetzt.
Lebenserwartung
Wie wirkt sich STXBP1-Mutation auf die durchschnittliche Lebenserwartung aus?
Bislang liegen keine Daten zur Lebenserwartung bei STXBP1-RD vor. Menschen mit STXBP1-RD können bis ins hohe Erwachsenenalter leben (der älteste bekannte Patient ist 60 Jahre alt), wobei je nach Verlauf der Epilepsie, Funktionsstatus und Begleiterkrankungen in jedem Alter unterschiedliche Komplikationen auftreten können.
STXBP1-assoziierte Erkrankungen zeigen eine große individuelle Variabilität in der Lebenserwartung. Zwar existiert keine heilende Therapie, doch die Lebenserwartung ist nicht zwangsläufig stark verkürzt und hängt maßgeblich vom Schweregrad der Epilepsie, Begleiterkrankungen und dem allgemeinen Gesundheitszustand ab. Todesursachen umfassen Epilepsie-bedingte Ereignisse wie Status Epilepticus oder Sudden Unexpected Death in Epilepsy (Sudep) sowie Atemwegskomplikationen und andere Begleiterkrankungen.
Aufgrund des breiten Spektrums der Erkrankung (phänotypische Variabilität) gibt es keine allgemeingültige Aussage zur Lebenserwartung; sie ist individuell zu betrachten. Fortschritte in der medizinischen Versorgung und Behandlung (z.B. bessere Anfallskontrolle, Präventionsstrategien für Lungeninfektionen) können die Lebensqualität und potenziell auch die Lebenserwartung verbessern.
Erste Hinweise legen nahe, dass STXBP1 möglicherweise auch in Glia-Zellen eine Rolle spielen könnte. Bisher gibt es vorläufige Vermutungen, gestützt durch eine einzige Studie. Gliazellen spielen eine Rolle bei Atemwegserkrankungen.
STXBP1-Mutationen stehen in Zusammenhang mit einem höheren Risiko für Lungenprobleme bei Patienten, was wahrscheinlich auf eine beeinträchtigte Zilienfunktion zurückzuführen ist. In der Studie wird untersucht, wie STXBP1 die Zilienstruktur und die Bewegung von Schleim und Flüssigkeit in den Atemwegen beeinflussen könnte, die für die Gesundheit der Atemwege unerlässlich sind.
Behandlung
Welche Behandlungen gibt es gegen STXBP1-bezogene Symptome?
STXBP1–bedingte Epilepsie ist oft therapieresistent und erfordert eine individuelle, multidisziplinäre Behandlung. Über die Antiepileptika der ersten Wahl hinaus können breit wirksame Wirkstoffe mit sorgfältiger Dosierung in Betracht kommen, die auf die Art der Anfälle und die individuellen Faktoren des Patienten zugeschnitten sind. Bei refraktären Fällen kann unter metabolischer Überwachung eine ketogene Diät in Betracht gezogen werden. Zu den neuen Ansätzen gehören die Präzisionsmedizin auf der Grundlage genetischer und funktioneller Daten sowie die Teilnahme an klinischen Studien. Die VNS (Vagusnervstimulation) ist eine chirurgische Option für medikamentenresistente Epilepsie und kann in einigen STXBP1–Fällen helfen, wenn Medikamente nicht ausreichen. Eine Beurteilung ist in einem spezialisierten Zentrum erforderlich. Die ACTH–Therapie (Adrenocorticotropes Hormon) ist eine Kurzzeittherapie, die hauptsächlich bei bestimmten infantilen oder schweren pädiatrischen Epilepsien eingesetzt wird. Sie kann in bestimmten Fällen in Betracht gezogen werden, ist in der Regel nur in begrenzter Zeit anwendbar und erfordert eine individuelle Beurteilung in einem spezialisierten Epilepsiezentrum.
Da es zurzeit keine heilende Therapie gibt, konzentriert sich die Behandelung auf die Linderung der spezifischen Symptome durch medikamentöse Behandelung, sowie eine ganzheitliche therapeutische Förderung durch Physiotherapie, Logopädie, Ergotherapie, Frühförderung und Reha-Maßnahmen.
Forschung
Welche aktuellen Forschungsansätze gibt es derzeit zu STXBP1?
Präklinische Studien, Natural-History-Studien und Patientenregister unterstützen die Vorbereitung auf klinische Studien. Diese Vorarbeiten dienen der Evidenzgenerierung, der Sicherheitseinschätzung und der Optimierung von Interventionen vor umfassenden klinischen Prüfungen. Sie erleichtern die Planung weiterer klinischer Studien, helfen dabei, Wirksamkeit und Sicherheit zu beurteilen, sowie optimale Vorgehensweisen festzulegen, bevor neue Therapien in größerem Maßstab getestet werden.
Die Forschung zu STXBP1 ist wichtig, weil sie zur Verbesserung der Diagnostik beiträgt. Durch größere Datensammlungen lässt sich variantenspezifisch schneller zwischen pathogen, wahrscheinlich pathogen und VUS unterscheiden. Erkenntnisse über die zugrunde liegenden Mechanismen der STXBP1-assoziierten Störung (STXBP1-RD) können zu zielgerichteten Therapien führen.
Drug Repurposing für STXBP1
Inwieweit kann Drug Repurposing oder gezielte Wirkstoffentwicklung neue Behandlungsoptionen für STXBP1-Retriktionen eröffnen?
Drug Repurposing für seltene Erkrankungen zielt darauf ab, vorhandene Arzneimittel neue Indikationen zuzuordnen, um Behandlungsoptionen für Patientinnen und Patienten mit seltenen Erkrankungen zu erweitern. Da die patientenbasierte Evidenzbasis oft begrenzt ist und die Entwicklungskosten für seltene Erkrankungen pro Patient stark ins Gewicht fallen, bietet die Umwidmung etablierter Moleküle einen potenziell schnelleren und kostengünstigeren Weg zur klinischen Anwendung.
Durch die Nutzung bereits vorhandener Sicherheits- und Toxizitätsdaten können frühe präklinische Schritte beschleunigt oder teilweise übersprungen werden, sodass der Übergang in spätere klinische Studien zügiger erfolgen kann.
KI- und Machine-Learning-Verfahren spielen hierbei eine zunehmende Rolle: Sie helfen, Muster in bestehenden Wirkstoffdatenbanken zu erkennen, potenzielle neue Indikationen zu ranken, synergistische Kombinationen zu identifizieren und so die Erfolgschancen bei seltenen Erkrankungen zu erhöhen. Zusätzlich erleichtert Repurposing die Erreichung regulatorischer Anforderungen, da dokumentierte Sicherheit bereits vorhanden ist, was den Weg zu Phase-II- oder Phase-III-Studien in vielen Fällen erleichtert. Insgesamt bietet Drug Repurposing für seltene Erkrankungen eine vielversprechende Strategie, um raschere, risikoärmere und kosteneffizientere Therapielösungen zu entwickeln, die direkt auf eine oft dringend benötigte Patientenversorgung abzielen.
Hoffnung für STXBP1-RD
Welche aktuellen Forschungsrichtungen bringen Hoffnung für STXBP1-RD
Die Forschung zu STXBP1 umfasst mehrere Pipelines, die sich auf das Verständnis der Erkrankung, die Entwicklung von Therapien und die Verbesserung der Lebensqualität der Betroffenen konzentrieren.
Die Rolle von STXBP1 bei Erkrankungen wurde erst 2008 entdeckt. Trotz der Neuheit und Seltenheit der Erkrankung schreitet die Forschung rasch voran. In den Jahren 2020 bis 2022 wurden ein Krankheitskonzeptmodell entwickelt und mehrere Studien zur natürlichen Krankheitsgeschichte durchgeführt; zudem begann eine frühe klinische Studie zu 4-Phenylbutyrat. Ende 2022 befanden sich mehr als neun potenzielle Therapien für STXBP1-Erkrankungen in der Entwicklung. Die Therapie-Pipeline für STXBP1-Erkrankungen wird kontinuierlich erweitert. Im vierten Quartal 2025 befinden sich mehr als 20 potenzielle Therapien in der Entwicklung; zwei dieser Therapien wurden als Orphan-Arzneimittel ausgewiesen. Zu den Pipelines gehören repurposed drugs bzw. kleine Moleküle, Gentherapie (Genersatztherapie und CRISPRa) und RNA-Therapie (ASOs, RNA-Interacting Tech, SINEUP und Arginine-Read-Through).
Einige Pipelines befinden sich bereits in präklinischen Studien, ebenso wie es bereits klinische Studien mit 4-Phenylbutyrat, Bexicaserin, Relutrigine und ß-MNM gibt. Darüber hinaus gibt es Naturgeschichts- und Registerstudien sowie weitere Beobachtungsstudien. In einer Beobachtungsstudie wird eine Person oder Gruppe ohne jegliche Intervention beobachtet. Eine Naturgeschichtsstudie untersucht, wie sich eine Krankheit im Verlauf der Zeit in einer Patientenpopulation verändert. Ein Patientenregister ist ein organisiertes System zur Erfassung, Speicherung und Verbreitung von Informationen über Menschen, die an einer Krankheit leiden.
Informieren Sie sich regelmäßig auf der Webseite über Fortschritte in der STXBP1-Gentherapie und weitere klinische Studien.
Internationale STXBP1-RD-Kooperation
Welche internationalen Partnerschaften fördern STXBP1-RD-Forschung und -Therapieentwicklung?
Die Zusammenarbeit in Deutschland beginnt mit der Einbindung der STXBP1 Foundation (USA), um ein solides Verständnis der Genotyp-Phänotyp-Beziehungen bei STXBP1-RD zu erlangen. Zu den Partnern gehören weiterhin das European STXBP1 Consortium (ESCO) und EU-Labore wie z. B. die VU Amsterdam, um gemeinsame klinische Studien durchzuführen und standardisierte Protokolle zu entwickeln. Zu den Vorteilen gehören eine beschleunigte Diagnostik, klarere Genotyp-Phänotyp-Korrelationen, Zugang zu internationalen Studien, Biobanken und neuartigen Therapien sowie die Entwicklung evidenzbasierter Behandlungen und eine verstärkte Unterstützung der Familien durch transparente Kommunikation und Netzwerke. Durch die Zusammenarbeit soll die Forschung vorangetrieben, der Zugang zu Ressourcen erweitert und neue Hoffnung auf bessere Ergebnisse für STXBP1-RD-Patienten weltweit geweckt werden.
Außerdem werden Biomarker-Ansätze verstärkt untersucht, um die Diagnostik zu verbessern, den Krankheitsverlauf besser abzubilden und die Reaktion auf Therapien zu überwachen. Dazu zählen genetische und proteomische Marker, bildgebende Indikatoren sowie funktionelle Biomarker, die STXBP1-bezogene Synapsenaktivität widerspiegeln.
Geschichte: Entdeckung des Gens STXBP1
Welche historischen Meilensteine gab es bei der Entdeckung des Gens STXBP1?
STXBP1-RD steht für STXBP1-Related Disorders (TXBP1-assoziierte Störungen). Die Genvariante wird auch als "Munc18-1" bezeichnet. Das STXBP1-Gen und die damit verbundenen Erkrankungen wurden im Jahr 2008 entdeckt, als Studien mit Personen durchgeführt wurden, die an einer schweren frühkindlichen Epilepsie, dem sogenannten Ohtahara-Syndrom, litten. Allerdings entdeckte Prof. Dr. Matthijs Verhage schon im Jahr 2000, dass das Protein Syntaxin1 für die Neurotransmission bei STXBP1 unerlässlich ist. Seit dieser Erstentdeckung hat sich das Verständnis der STXBP1-assoziierten Störungen erweitert. Neben Othahara-Syndrom können STXBP1-Varianten auch West-Syndrom verursachen. West-Syndrom ist eine schwere Epilepsieform, die meist im ersten Lebensjahr auftritt und gekennzeichnet ist durch Hypsarrhythmie im EEG.